新英格蘭醫(yī)學雜志:康諾亞自主研發(fā)CM336(BCMAxCD3雙抗)在治療自身免疫性溶血性貧血中顯示優(yōu)異療效
公司要聞
?2025年06月12日
2025年6月11日,中國醫(yī)學科學院血液病醫(yī)院(中國醫(yī)學科學院血液學研究所)施均教授團隊在《New England Journal of Medicine》期刊(新英格蘭醫(yī)學雜志,IF=96.3)在線發(fā)布了題為“BCMA-Targeted T-Cell Engager for Autoimmune Hemolytic Anemia after CD19 CAR T-Cell Therapy”的研究成果1。該研究首次報告了2例接受自體CD19 CAR-T細胞治療后再次復發(fā)的多線治療失敗的自身免疫性溶血性貧血(AIHA)患者,通過康諾亞自主研發(fā)的CM336(BCMA x CD3雙抗)挽救治療成功。該研究結果表明,CM336在治療嚴重的復發(fā)/難治性自身免疫性溶血性貧血中展現(xiàn)出優(yōu)異的初步療效和安全性,有望成為AIHA等自身免疫性疾病的革新型治療方案。

圖源:《新英格蘭醫(yī)學雜志》發(fā)表文章
自身免疫性溶血性貧血(AIHA)發(fā)病率高(1.8-3.0/10萬人年)、患病率高(17/10萬人),難治/復發(fā)患者占比高。約50%的患者經一線糖皮質激素、二線CD20單克隆抗體及多種常規(guī)免疫抑制劑治療后,出現(xiàn)多輪次的復發(fā)且不能擺脫藥物依賴。疾病影響患者生活質量,患者常有血栓形成、嚴重感染、股骨頭壞死等,致殘、殘死風險高達10-30%,臨床亟需創(chuàng)新治療突破。
該研究中,2例AIHA患者在接受CM336治療前已接受過包括糖皮質激素、脾切除術、抗CD20抗體、BTK抑制劑和CD19 CAR-T細胞療法等多種治療,但疾病仍最終復發(fā)或進展為難治。
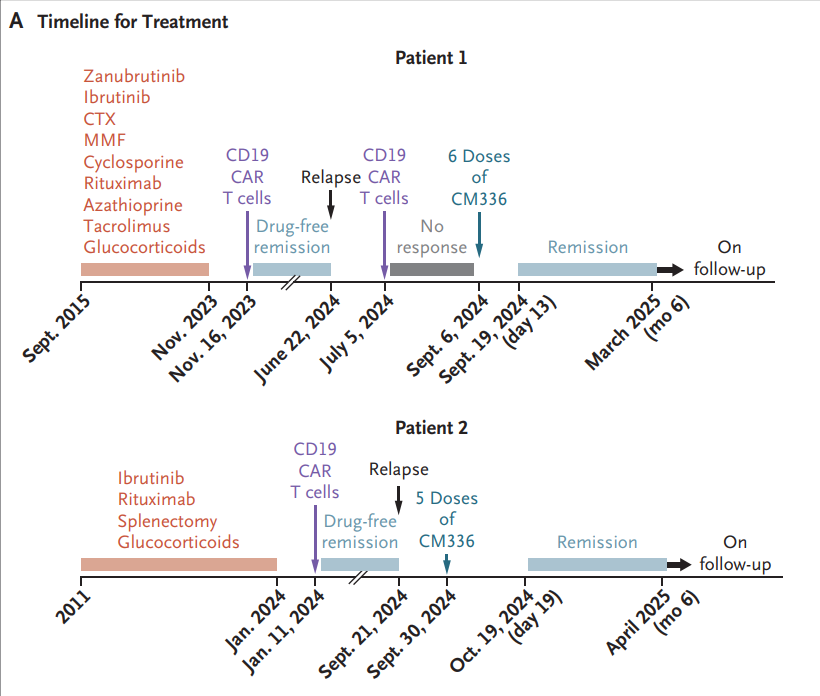
圖:患者治療情況(《新英格蘭醫(yī)學雜志》發(fā)表文章)
研究結果顯示1,2例患者在接受CM336治療后溶血明顯改善:
■ 第1例患者在第13天達部分緩解,第17天血紅蛋白水平恢復正常;第2例患者在第19天達部分緩解,第21天達完全緩解,治療期間未接受其他藥物治療。
■ 2例患者溶血指標(網(wǎng)織紅細胞百分比、乳酸脫氫酶、間接膽紅素)均明顯下降,并維持至隨訪6個月持續(xù)處于無治療緩解中。
■ 不良反應僅觀察到1級皮膚硬結及低丙球蛋白血癥,未見其他嚴重不良反應,未發(fā)生細胞因子釋放綜合征(CRS)、免疫效應細胞相關神經毒性綜合征(ICANS)或感染事件,整體安全性良好。
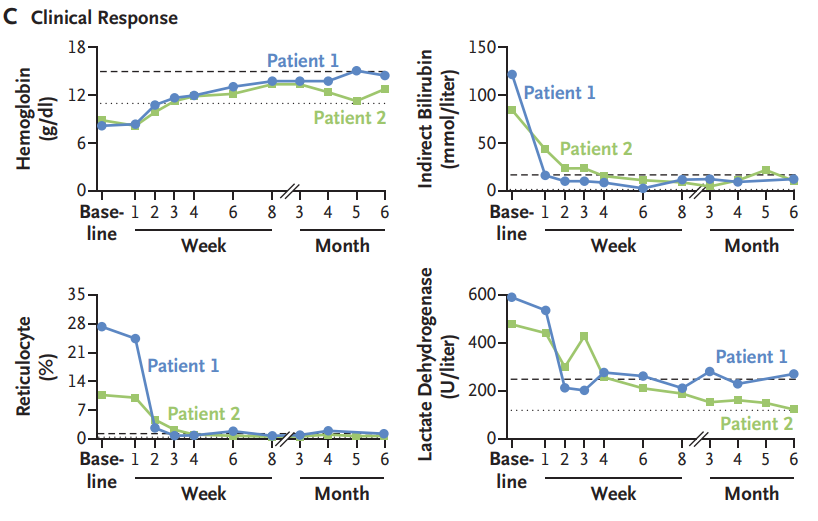
圖:CM336治療后臨床效果(《新英格蘭醫(yī)學雜志》發(fā)表文章)
研究整體顯示,CM336在治療既往接受過多種治療的復發(fā)/難治性自身免疫性溶血性貧血患者中表現(xiàn)出令人驚喜的初步療效,患者病情能夠得到快速控制且可達到半年以上的持續(xù)緩解,同時安全性良好。
本研究首次展示了BCMA x CD3雙抗在CD19 CAR-T復發(fā)后的AIHA患者中獲得治療成功,表明BCMA靶點的治療不僅可以作為靶向CD19治療的挽救治療策略,也為常規(guī)免疫抑制劑二線治療失敗的AIHA患者開展靶向BCMA的臨床研究提供了依據(jù)。CM336有望為此類患者提供一種極具應用前景的新型治療選擇,為該疾病的治療帶來革新性改變。
康諾亞于2024年11月與Ouro Medicines Ltd(f/k/a Platina Medicines Ltd)訂立獨家許可協(xié)議,授予Ouro Medicines在全球(不包括中國內地、香港、澳門及臺灣地區(qū))研究、開發(fā)、生產、注冊及商業(yè)化CM336的獨家權利。基于此次《新英格蘭醫(yī)學雜志》發(fā)表的積極研究數(shù)據(jù),Ouro Medicines計劃于2025年下半年啟動針對該疾病的臨床研究,并計劃于2025年6月14日歐洲血液學協(xié)會(EHA)年會以海報形式報告CM336相關數(shù)據(jù),重點介紹其在復發(fā)/難治性多發(fā)性骨髓瘤試驗中的安全性與療效數(shù)據(jù),及其在自身免疫性血細胞減少癥中的潛在應用。
同時,康諾亞正加速推進CM336在國內的臨床開發(fā),用于治療原發(fā)性輕鏈型淀粉樣變性的II期臨床研究已獲得國家藥品監(jiān)督管理局藥品審評中心批準;用于治療自身免疫性血細胞減少癥的臨床研究也在積極準備中,通過加速推進多種適應癥研究,進一步提升該候選藥物的開發(fā)進度和未來潛力。
備注:
1. Zhang L, Gao Z, Pan H, et al. BCMA-Targeted T-Cell Engager for Autoimmune Hemolytic Anemia after CD19 CAR T-Cell Therapy. N Engl J Med. 2025 Jun 11;392:2282-2284.
